中学校では、「化学反応式の作り方・書き方」を学習しますが、完璧に理解できてますでしょうか?
この記事では、「化学反応とは」「化学反応式の作り方・書き方」についてわかりやすく解説しています。
それでは早速、「化学反応式の作り方・書き方」について一緒にがくしゅうしていきましょう!
【はじめに】自己紹介
このサイトは、現役の中学教師である「たつや」が管理・運営しています。
このサイトは、教師である私が「より多くの人に科学の面白さを知ってもらいたい!」「中学生が理科を好きになるようなサイトをつくりたい!」という思いのもと執筆しています。
私の簡単な自己紹介はこちらです!
 |
| 現役の中学校教師 理科教育歴 5年 理科の中でも「生物」が大好き! サイト運営 2021年7月~ 座右の銘は「不言実行」 |
まだまだ発展途上のサイトで、至らない点も多くあるかと思いますが、これからも「かめのこブログ」をよろしくお願いいたします(^○^)
私の詳しいプロフィールはこちらから!
0. 「化学変化」の記事 一覧
「化学変化」の単元に関係する記事の一覧です!
今、学習している内容がどこにあたるか確認しておきましょう!
1. 化学反応とは
① 化学反応とは
「化学反応」は、「化学変化」ともいわれます。
「化学反応」では、物質が別のの物質と反応したり、別の物質に分解したりします。
「化学反応」は、「化学反応式」を使って表すことができます。
② 化学反応の種類
「化学反応」には、大きく分けて「化合」「分解」「還元」「中和」などの種類があります。
種類ごとの特徴は次のとおりです。
●化合 … 2つ以上の物質が結合し、別の物質ができること。
| 化合の例 | 化学反応式 |
| 鉄と硫黄の化合 | Fe + S → FeS (鉄 + 硫黄 → 硫化鉄) |
| 銅の酸化 | 2Cu + O₂ → 2CuO (銅 + 酸素 → 酸化銅) |
| マグネシウムの燃焼 | 2Mg + O₂ → 2MgO (マグネシウム + 酸素 → 酸化マグネシウム) |
化合の中には、物質が酸素と化合する「酸化」や物質が熱や光を発生させながら反応する「燃焼」という反応があります。
●分解 … 物質が2種類以上の別の物質に分かれること。
| 分解の例 | 化学反応式 |
| 酸化銀の分解 | 2Ag₂O → 4Ag + O₂ (酸化銀 → 銀 + 酸素) |
| 水の電気分解 | 2H₂O → 2H₂ + O₂ (水 → 水素 + 酸素) |
●還元 … 酸素を含む物質から酸素が取り除かれる反応。「酸化」の逆。
| 還元の例 | 化学反応式 |
| 酸化銅の還元(炭素) | 2CuO + C → 2Cu + CO₂ (酸化銅 + 炭素 → 銅 + 二酸化炭素) |
| 酸化鉄の還元(水素) | Fe₃O₄ + 4H₂ → 3Fe + 4H₂O (酸化鉄(Ⅲ) + 水素 → 鉄 + 水) |
●中和 … 酸性とアルカリ性の水溶液が混ざることで、水と塩(えん)ができる反応のこと。(詳しくは中3で勉強します!)
| 中和の例 | 化学反応式 |
| 塩酸と水酸化ナトリウム | HCl + NaOH → NaCl + H₂O (塩酸 + 水酸化ナトリウム → 塩化ナトリウム + 水) |
| 硫酸と水酸化バリウム | H₂SO₄ + Ba(OH)₂ → BaSO₄ + 2H₂O (硫酸 + 水酸化バリウム → 硫酸バリウム + 水) |
2. 化学反応式の作り方・書き方
化学反応式の作り方・書き方の手順は次のとおりです!
① 日本語で式を書く
② 日本語を化学式に直す
③ 式の左右の元素の数を確認する
④ 係数で式の左右の元素の数を合わせる
今回は、「スチルウール(鉄)の燃焼」を例に、化学反応式の作り方を確認していきます!
① 日本語で式を書く!
まずは、日本語で式を書きます。
「スチルウール(鉄)」は、火をつけると、「酸素」と反応して、「酸化鉄」になります。
鉄 + 酸素 → 酸化鉄
日本語で式を立てるときの注意点は次の2つです。
・数式と同じく、左から右に書く。
・化学反応式では、「=」ではなく「→」を使う。
② 日本語を化学式に直す!!
次は日本語を「化学式」に変えていきましょう。
「鉄」「酸素」「酸化鉄」は化学式で書くと、次のようになります。
鉄 → Fe
酸素 → O₂
酸化鉄 → FeO
したがって、日本語を化学式に置き換えると次のようになります。
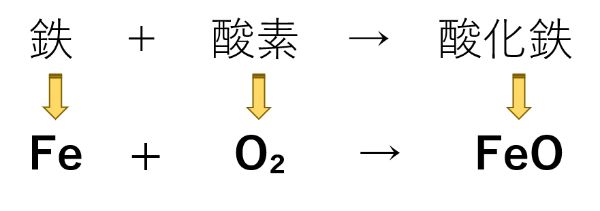
この時の注意点は次のとおりです。
・「酸素」は、自然の中では2つがくっついた分子の状態で存在します。そのため、「O」ではなく、「O₂」と書きます。
③ 式の左右の原子の数を数える!!!
次に、式の左右の原子の数を数えます。
式の中に出てくる化学式を原子や分子の形で表すと次のようになります。
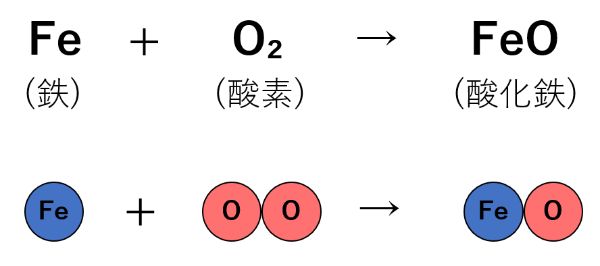
原子の数をまとめると、、
式の左側 → 鉄(Fe)の原子 1つ、酸素(O2)の原子 2つ
式の右側 → 鉄(Fe)の原子 1つ、酸素(O2)の原子 1つ
このようになり、鉄の原子の数は同じですが、酸素の原子の数が足りていません。
式の左側と右側で原子の数は同じでなければならないため、このままでは正しい化学反応式とは言えません。
④ 係数で式の左右の原子の数を合わせる!!!!
最後は、係数で原子の数を合わせます。
係数を書く時の鉄則は「原子の数が足りないを増やすこと」です。
先ほどの化学反応式を確認すると、式の右側の「酸素の原子(O)」の数が足りないことが分かります。
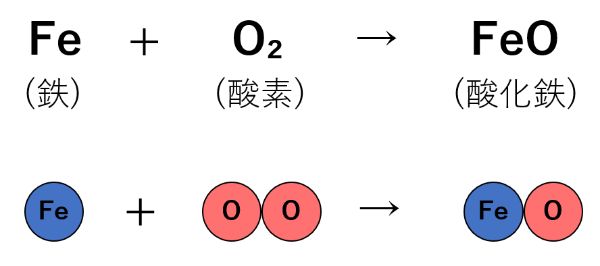
したがって、式の右側の「酸素の原子(O)」の数を増やすために、「酸化鉄(FeO)」の前に係数の「2」を書きます。
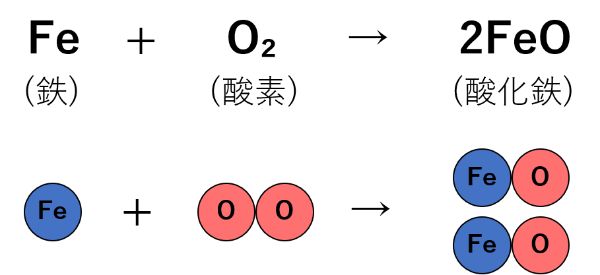
そうすると、式の右側の「Fe」と「O」が1つずつ増え、今度は式の右側の「鉄の原子(Fe)」の数が足りなくなります。
したがって、次は左側の「鉄の原子(Fe)」の数を増やすために、「鉄(Fe)」の前に係数の「2」を書きます。
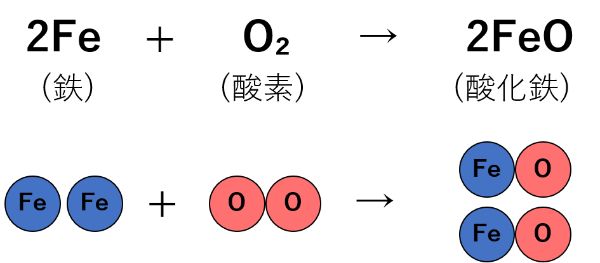
これで式の右側と左側の原子の数をそろえることができました!!
お疲れさまでした。これで、正しい化学反応式の完成です。
このように、足りない部分を増やしていくことで、式の左側と右側の原子の数を合わせることができます。
3. まとめ
今回は、「化学反応式の作り方・書き方」について学習していきました。
化学反応式は、これから中学校だけでなく、高校でもとても大切になってくるので、必ずマスターしておきましょう。
最後まで読んでいただきありがとうございました!!
またね~!

















