中学校で学習する「原子」と「分子」の違いはよく理解できていますか?
この記事では、「原子・分子の違い」「原子で存在する物質」「分子で存在する物質」などについて解説しています。
それでは早速、「原子・分子の違い」について一緒に学習していきましょう!
【はじめに】自己紹介
このサイトは、現役の中学教師である「たつや」が管理・運営しています。
このサイトは、教師である私が「より多くの人に科学の面白さを知ってもらいたい!」「中学生が理科を好きになるようなサイトをつくりたい!」という思いのもと執筆しています。
私の簡単な自己紹介はこちらです!
 |
| 現役の中学校教師 理科教育歴 5年 理科の中でも「生物」が大好き! サイト運営 2021年7月~ 座右の銘は「不言実行」 |
まだまだ発展途上のサイトで、至らない点も多くあるかと思いますが、これからも「かめのこブログ」をよろしくお願いいたします(^○^)
私の詳しいプロフィールはこちらから!
0. 「物質のなりたち」の記事 一覧
「物質のなりたち」の単元に関係する記事の一覧です!
今、学習している内容がどこにあたるか確認しておきましょう!
1. 【結論】原子・分子の違い
① 原子・分子の違い
まずは、ざっくりと「原子」と「分子」の違いを理解しましょう!
〇 原子 … 小さな1つの粒のこと。物質の最小単位。
〈例〉水素原子(H)、酸素原子(O)など
〇 分子 … 原子が2つ以上くっついたもの。
〈例〉水素分子(H₂)、水分子(H₂O)など
② 原子の例
原子は、今のところ118種類あることが分かっています。
主な原子の例は、次の通りです。
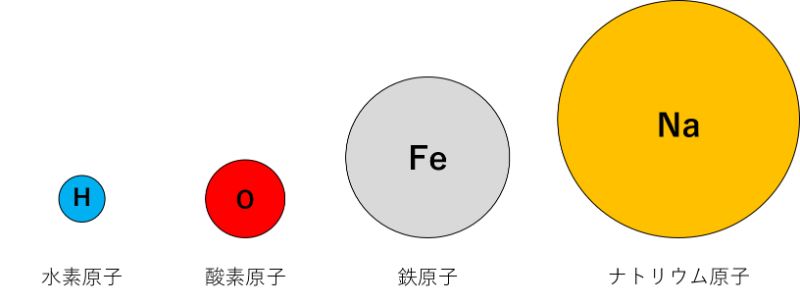
原子は、種類によって大きさが違います。上の図は、大体の原子の大きさの違いを表しています。
すべての物質は、この「原子」が集まってできています。そのため、原子は「物質の最小単位」ということができます。
③ 分子の例
「分子」は、原子が2つ以上くっついたもののことです。
例えば、2つの「水素原子(H)」がくっつくと、「水素分子(H₂)」になります。
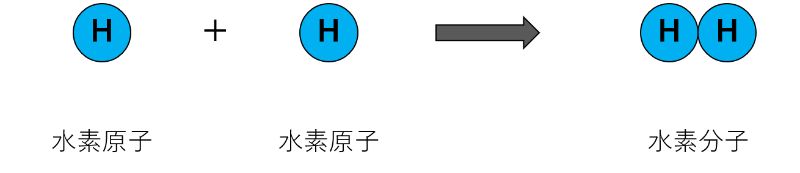
また、2つの「水素原子(H)」と1つの「酸素原子(O)」がくっつくと、「水分子(H₂O)」となります。
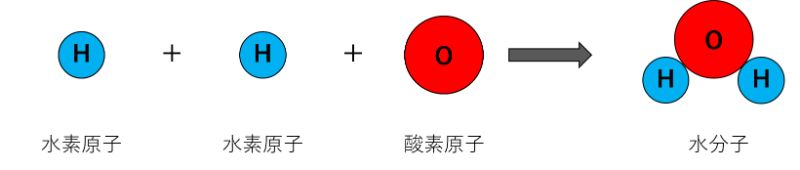
このように、原子が2つ以上くっついたものを「分子」といます。
2. 原子(げんし)
「原子」は、「小さな1つの粒のこと。物質の最小単位。」でした。
物質によって、常温・常圧(普段生活している環境)で「原子」の状態で存在しているか、「分子」の状態で存在しているかが決まっています。
どんな物質が、「原子」の状態で存在しているのか確認してみましょう!
① 原子で存在する物質
中学生の段階で、覚えてほしい「原子」の状態で存在する物質は、次の通りです。
たくさんありますが、全体をみると、「固体」や「金属」「貴ガス」など共通点がみえてくると思います。
| 物質名 | 化学式 | 常温・常圧での状態 | 備考 |
|---|---|---|---|
| ヘリウム | He | 気体 | 貴ガス |
| 炭素 | C | 固体 | |
| ナトリウム | Na | 固体 | 金属 |
| マグネシウム | Mg | 固体 | 金属 |
| アルミニウム | Al | 固体 | 金属 |
| 硫黄 | S | 固体 | |
| マンガン | Mn | 固体 | 金属 |
| 鉄 | Fe | 固体 | 金属 |
| 亜鉛 | Zn | 固体 | 金属 |
| アルゴン | Ar | 気体 | 貴ガス |
| 銀 | Ag | 固体 | 金属 |
| 白金(プラチナ) | Pt | 固体 | 金属 |
| 金 | Au | 固体 | 金属 |
| 水銀 | Hg | 液体 | 金属 |
これらの物質は、「原子」の状態で、自然界に存在しています。
これらの物質をすべて覚える必要はありませんが、「化学式」を覚えるうえで大切になるので、ポイントを2つだけお伝えしておきます!
(1)「固体」の単体は、原子で存在する。
(2)「気体」や「液体」でも一部原子で存在するものがある。
(1)「固体」の単体は、原子で存在する
基本的に常温・常圧(普段生活している環境)で、「固体」の状態で存在する物質は、「原子」の形で存在しています。
代表的なものには「金属」が多いですが、「炭素(C)」や「硫黄(S)」も固体なので、原子の形で存在しています。
(2)「気体」や「液体」でも一部原子の形で存在する
「気体」や「液体」で、自然界で原子の形をとっているものは、あまり多くはありませんが、次の3つだけは覚えておきましょう。
まずは、「ヘリウム(He)」「アルゴン(Ar)」です。
この2つは、「貴(き)ガス」と呼ばれる物質のグループに属しています。
「貴ガス」とは、周期表の一番右にある物質のことです。
「貴ガス」は、「気体」の状態でも原子の形で存在しているという特徴があります。
そのため、「化学式」を覚えるときには、「He₂」や「Ar₂」と書かないようにしましょう。
次は、「水銀(Hg)」です。
水銀は、常温・常圧で「液体」の珍しい金属です。
「金属」は、基本的に原子の形で存在するので、他の金属と一緒にまとめて覚えましょう。
ちなみに、原子番号35番の「臭素(Br)」は、常温・常圧で「液体」ですが、「Br₂」の状態で存在します。
いろいろな物質があって面白いですよね。
3. 分子(ぶんし)
「分子」は、「原子が2つ以上くっついたもの」のことでした。
「分子」のでき方には決まりがあります。
また、「分子」は、どの原子がくっつくかによって、その性質がガラリと変わるというとても面白い特徴があります。
「分子」について、もう少し詳しく勉強してみましょう!
① 分子のでき方の決まり
「分子」をつくることができる「原子」の組み合わせは決まっています。
詳しくは、高校の化学で勉強しますが、「どの原子でもくっつけるわけではない」ということは理解しておいてください!
例えば、「水素原子(H)」と「酸素原子(O)」は、「H」が2つと「O」が1つでくっつくことができ、「水(H₂O)」ができますね。
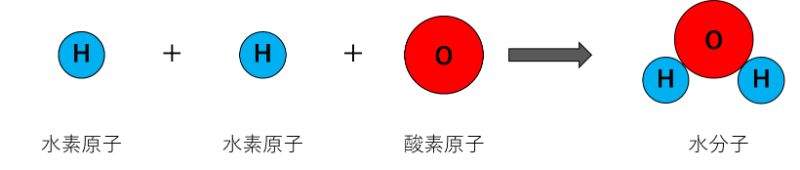
「水素原子(H)」と「酸素原子(O)」は、「水(H₂O)」の形ではくっつくことができますが、「H」と「O」を1つずつや2つずつくっつけることはできません。
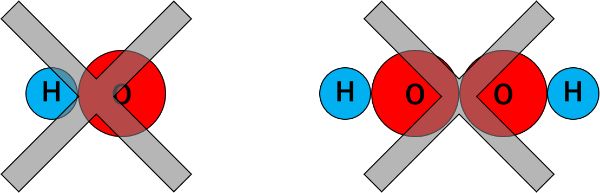
このように、「水素原子(H)」と「酸素原子(O)」だけをみてみても、くっつくことができる組み合わせは決まっているのです。
「水素原子(H)」と「酸素原子(O)」のくっつくことができる組合せには、次のようなものもあります。
| 物質名 | 水素分子 | 酸素分子 | 水 | オゾン |
| 化学式 | H₂ | O₂ | H₂O | O₃ |
| 性質 | とても軽い気体 気体が燃える | 気体 物を燃やす | 液体 | くさい気体 有毒 |
分子の つくり | 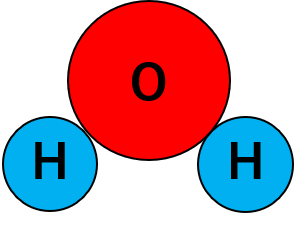 | 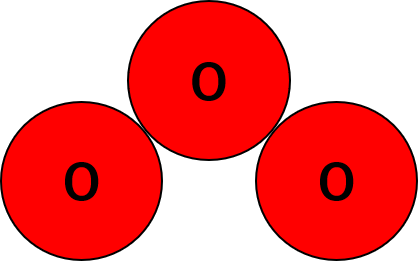 |
② 分子で存在する物質
常温・常圧(普段生活している環境)で、「分子」の形で存在している物質には、次のようなものがあります。
| 物質名 | 化学式 | 常温・常圧での状態 |
|---|---|---|
| 水素 | H₂ | 気体 |
| 窒素 | N₂ | 気体 |
| 酸素 | O₂ | 気体 |
| 塩素 | Cl₂ | 気体 |
| 水 | H₂O | 液体 |
| アンモニア | NH₃ | 気体 |
| 酸化銅 | CuO | 固体 |
| 水酸化ナトリウム | NaOH | 固体 |
| 塩化ナトリウム | NaCl | 固体 |
| 塩化水素 | HCl | 気体 |
| 硫化鉄 | FeS | 固体 |
| 炭酸水素ナトリウム | NaHCO₃ | 固体 |
| 炭酸ナトリウム | Na₂CO₃ | 固体 |
このように、「分子」で存在する物質には、1種類の元素からできている「単体」より2種類以上の元素からできている「化合物」が多いです。
また、「単体」では、「酸素(O₂)」や「窒素(N₂)」など主に「気体」の物質が分子の形で存在しています。
4. まとめ
今回は、「原子と分子の違い」について解説していきました。
最後に、この記事のポイントをおさらいしておきましょう!
① 「原子」は、「小さな1つの粒。物質の最小単位」のこと。
② 「分子」は、「原子が2つ以上くっついたもの」のこと。
③ 原子で存在するものには、「常温・常圧で固体で存在する物質」や「金属」、「貴ガス」などがある。
④ 分子で存在するものには、「単体の気体」や「化合物」がある。
⑤ 分子は、なんの原子が組み合わさるかによって、性質がガラリと変わる。
最後まで読んでいただき、ありがとうございました!
















