中学校の理科では、「再結晶」について学習しますが、よく理解できていますか?
この記事では「再結晶とは」「再結晶の例」などをわかりやすく解説しています。
それでは早速「再結晶」について一緒に学習していきましょう!
1. 再結晶とは
「再結晶(さいけっしょう)」とは、溶解度の差を利用して液体の中の物質を取り出す作業のことです。
再結晶をすることで、不純物を取り除き、物質の純度を高めることができます。
2. 再結晶の例
再結晶には、大きく分けて2つの方法があります。
それは、「溶媒を蒸発させる方法」と「温度の差を利用する方法」です。
それぞれ簡単に紹介していきます(^O^)/
① 溶媒を蒸発させる方法
1つ目は、「溶媒を蒸発させる方法」です。
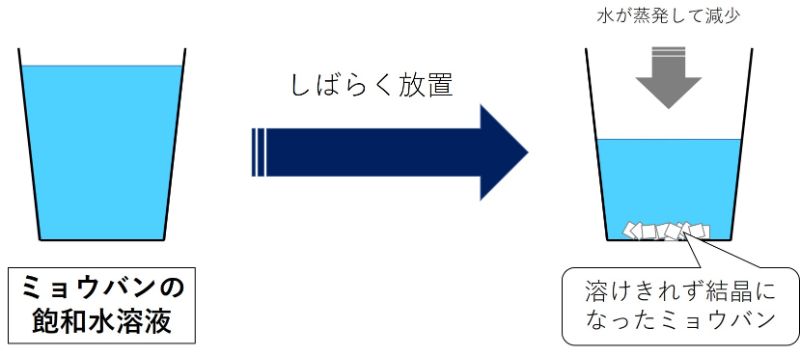
ミョウバンを水にできるだけ溶かし、ミョウバン水溶液をつくります。
このミョウバン水溶液をしばらく放置しておくと、だんだん水が蒸発して溶けきれなくなったミョウバンが再結晶します。
② 温度の溶解度の差を利用した方法
続いては、「温度の溶解度の差を利用した方法」です。
水の温度や量によって、物質の溶ける量は決まっています。100gの水に溶ける物質の量を「溶解度」といいます。
ミョウバンの溶解度と温度の関係は下のとおりです。
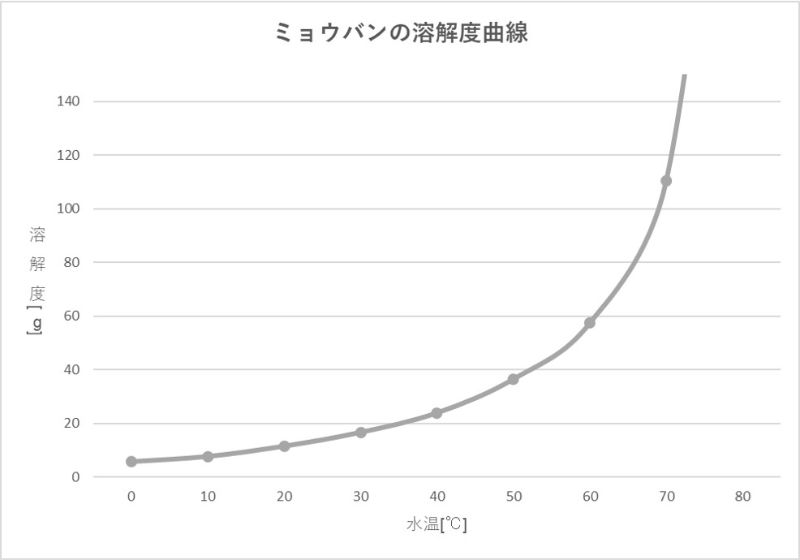
このように、ミョウバンは温度が高ければ高いほど水にたくさん溶けます。
「溶解度」についてより詳しく知りたい人は下の記事も参考にしてください。

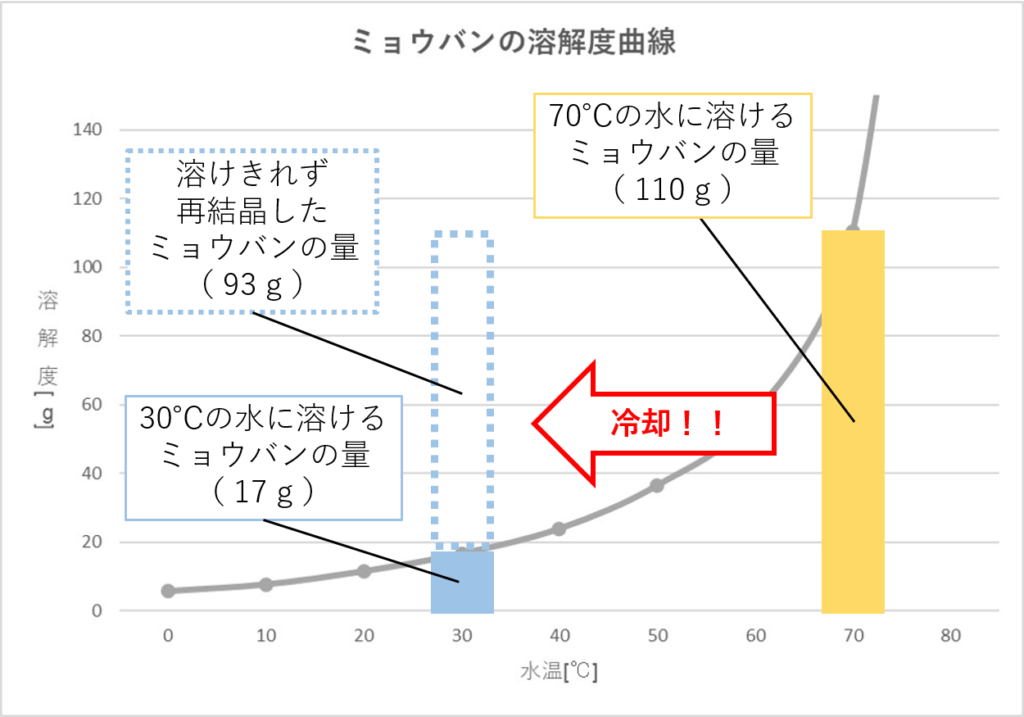
70℃の熱湯にミョウバンをできるだけ溶かしたミョウバン水溶液をつくり、それを冷やして30℃にする場合について考えてみましょう。
70℃の水に溶けるミョウバンの量は「約110g」です。
一方で、30℃の水に溶けるミョウバンの量は「約17g」です。
そのため、70℃から30℃までミョウバン水溶液を冷やすと、「110 - 17 = 93 [g] 」のミョウバンが結晶として取り出せます。